Выяснит для чего нужен анион и катион. Анионы и катионы
В волшебном мире химии возможно любое превращение. Например, можно получить безопасное вещество, которым часто пользуются в быту, из нескольких опасных. Подобное взаимодействие элементов, в результате которого получается однородная система, в которой все вещества, вступающие в реакцию, распадаются на молекулы, атомы и ионы, называется растворимость. Для того чтобы разобраться с механизмом взаимодействия веществ, стоит обратить внимание на таблицу растворимости .
 Таблица, в которой показана степень растворимости, является одним из пособий для изучения химии. Те, кто постигают науку, не всегда могут запомнить, как определённые вещества растворяются, поэтому под рукой всегда следует иметь таблицу.
Таблица, в которой показана степень растворимости, является одним из пособий для изучения химии. Те, кто постигают науку, не всегда могут запомнить, как определённые вещества растворяются, поэтому под рукой всегда следует иметь таблицу.
Она помогает при решении химических уравнений, где участвуют ионные реакции. Если результатом будет получение нерастворимого вещества, то реакция возможна. Существует несколько вариантов:
- Вещество хорошо растворяется;
- Малорастворимо;
- Практически не растворяется;
- Нерастворимо;
- Гидрализуется и не существует в контакте с водой;
- Не существует.
Электролиты
Это растворы или сплавы, проводящие электрический ток. Электропроводность их объясняется мобильностью ионов. Электролиты можно поделить на 2 группы :
- Сильные. Растворяются полностью, независимо от степени концентрации раствора.
- Слабые. Диссоциация проходит частично, зависит от концентрации. Уменьшается при большой концентрации.
 Во время растворения электролиты диссоциируют на имеющие разный заряд ионы: положительные и отрицательные. При воздействии тока положительные ионы направляются в сторону катода, тогда как отрицательные в сторону анода. Катод – положительный заряд, анод – отрицательный. В итоге происходит движение ионов.
Во время растворения электролиты диссоциируют на имеющие разный заряд ионы: положительные и отрицательные. При воздействии тока положительные ионы направляются в сторону катода, тогда как отрицательные в сторону анода. Катод – положительный заряд, анод – отрицательный. В итоге происходит движение ионов.
Одновременно с диссоциацией проходит противоположный процесс – соединение ионов в молекулы. Кислоты – это такие электролиты, при распаде которых образуется катион – ион водорода. Основания – анионы – это гидроксид ионы. Щелочи – это основания, которые растворяются в воде. Электролиты, которые способны образовывать и катионы и анионы, называются амфотерными.
Ионы
Это такая частица, в которой больше протонов или электронов, он будет называться анион или катион, в зависимости от того, чего больше: протонов или электронов. В качестве самостоятельных частиц они встречаются во многих агрегатных состояниях: газах, жидкостях, кристаллах и в плазме. Понятие и название ввёл в обиход Майкл Фарадей в 1834 году. Он изучал воздействие электричества на растворы кислот, щелочей и солей.
Простые ионы несут на себе ядро и электроны. Ядро составляет почти всю атомную массу и состоит из протонов и нейтронов. Количество протонов совпадает с порядковым номером атома в периодической системе и зарядом ядра. Ион не имеет определённых границ из-за волнового движения электронов, поэтому невозможно измерить их размеры.
Отрыв электрона от атома требует, в свою очередь, затрат энергии. Она называется энергия ионизации. Когда присоединяется электрон, происходит выделение энергии.
Катионы
Это частицы, носящие положительный заряд. Могут иметь разную величину заряда, например: Са2+ – двузарядный катион, Na+ – однозарядный катион. Мигрируют к отрицательному катоду в электрическом поле.
Анионы
Это элементы, имеющие отрицательный заряд. А также обладает различным количеством величины зарядов, например, CL- – однозарядный ион, SO42- – двухзарядный ион. Такие элементы входят в состав веществ, обладающих ионной кристаллической решёткой, в поваренной соли и многих органических соединениях.
- Натрий . Щелочной металл. Отдав один электрон, находящийся на внешнем энергетическом уровне, атом превратится в положительный катион.
- Хлор . Атом этого элемента принимает на последний энергетический уровень один электрон, он превратится в отрицательный хлорид анион.
- Поваренная соль . Атом натрия отдаёт электрон хлору, вследствие этого в кристаллической решётке катион натрия окружён шестью анионами хлора и наоборот. В результате такой реакции образуется катион натрия и анион хлора. Благодаря взаимному притяжению формируется хлорид натрия. Между ними образуется прочная ионная связь. Соли – это кристаллические соединения с ионной связью.
- Кислотный остаток . Это отрицательно заряженный ион, находящийся в сложном неорганическом соединении. Он встречается в формулах кислот и солей, стоит обычно после катиона. Практически для всех таких остатков есть своя кислота, например, SO4 – от серной кислоты. Кислот некоторых остатков не существует, и их записывают формально, но они образуют соли: фосфит ион.
Химия – наука, где возможно творить практически любые чудеса.
АНИОН — это отрицательно заряженная частица кислорода. Анион- это не искусственно выращенная частица в лабораторных условиях.
Анион, как ни странно присутствует в воздухе,и здоровье на прямую зависит от их количества. Анионы могут аккумулировать и нейтра лизовать пыль, уничтожать вирусы с положительно заряженными электронами, проникать в клетки бактерий и уничтожать их, пред отвращая таким образом негативные последствия для человеческо го организма. При ионизации человека отмечаются улучшения в ра боте всех органов и систем организма:
Сердечно сосудистой системы, нормализация артериального давления, центральной нервной системы, желудочно-кишечного тракта, мочеполовой системы и отмечается общее омоложение организма.
Особо большое скопление анионов присутствует в морском и горном воздухе. Наверняка Вы наблюдали, что возле моря Вам дышится легче и улучшается самочувствие. А про долгожителей горных поселений ходят легенды.
Каким образом анионы присутствуют в женских гигиенических прокладках? – спросите Вы?
В природе есть такой минерал — ТУРМАЛИН.
А это уже отшлифованные камни
Турмалин при определённых условиях (1.трение, 2.влага, 3.темпера тура) излучает анионы. Все три условия присущи человеческому ор ганизму.
Как лекари, турмалины положительно влияют на нервную систему, сон, эндокринную и иммунную системы. Уникальный минерал тур малин хорошо лечит кровеносную систему, воспроизводительную функцию организма.
Минерал нейтрализует отрицательные эмоции. Из всех зелёных камней турмалин имеет самые сильные омолаживающие качества.
Как камень нижних энергий прекрасно подходит как средство от половых расстройств, бессилия и пр. У мужчин укрепляет потенцию. Для низменных людей он может оказаться афродозиаком, сделав сексуальную энергию неуправляемой.
Очень любопытно, что турмалин считается сильным лечебным средством при онкологических заболеваниях. По некоторым данным, турмалины могут быть индикаторами радиоактивности, а кровь
онкологических больных обнаруживает очень специфическое излуче ние. При лечении турмалин кладут между чакрами для проводки энергии от одной чакры к другой. Особенно хорошо применять его с родохрозитом и малахитом на солнечное сплетение для объединения энергий.
Из всех существующих на земле минералов только турмалин несёт в себе постоянный электрический заряд, за что его и называют крис таллическим магнитом.
При нагревании турмалин создаёт низкочастотное магнитное поле, излучает анионы, которые действуют на человеческий организм следующим образом:
· Усиливается клеточный метаболизм, улучшается обмен веществ;
· Улучшается местный кровоток;
· Восстанавливается работа лимфатической системы;
· Восстанавливаются эндокринная и гормональная системы;
· Улучшается питание в органах и тканях;
· Укрепляется иммунитет;
· Содействуют уравновешенности вегетативной системы(это система возбуждения и торможения психики);
· Обеспечениие организма живительной энергией;
· Улучшается качество крови, стимулируются кровообращение и разжижение крови,так что она поступает в тончайшие капилляры, придавая организму жизненных сил. Очищает сосуды, заряжает плазму.
· Применяются при болезнях печени;
· Улучшают сон;
· Восстанавливают нервы после стрессовых ситуаций;
· Улучшают цвет лица;
· Укрепляют потенцию и половую функцию организма;
· Улучшают зрение и память;
· Облегчают головные боли, снимают головокружение;
· Устраняют неприятные запахи, имеют антибактериальные свойства.
В проточной воде можно снять лишний заряд с камня. Для того, чтобы снова его зарядить – нужно немного подержать на солнце. Являясь природным минералом, турмалин не даёт побочных явлений.
Компания «ВИНАЛАЙТ», используя инновационные нанотехнологии, нашла способ обработки и измельчение турмалина, переплетая с волокнами хлопка. Таким образом создан анионовый вкладыш или чип (не электронный), который помещён в женскую гинекологическую прокладку «Love Moon».
Количество концентрации анионов в 1 см 3:
Возле водопадов 7000 — 8000 анионов
Возле моря 3000 — 6000 анионов
В горах 3000 — 5000 анионов
В лесах 700 — 1500 анионов
В городах 100 -200 анионов
В квартирах 25 -75 анионов
В анионовом вкладыше ~ 5800 анионов на 1 см3.
Человек, так же как и всякое другое живое существо, не может жить без анионов. А между тем, знаете ли Вы, что такое «анион»?В обычных условиях молекулы и атомы воздуха нейтральны. Однако при ионизации, которая может происходить посредством обычного излучения, ультрафиолетовой радиации, микроволновой радиации или же посредством простого удара молнии, молекулы воздуха теряют часть вращающихся вокруг атомного ядра отрицательно заряженных электронов, которые в дальнейшем присоединяются к нейтральным молекулам, придавая им отрицательный заряд. Такие молекулы мы и называем анионами.
У анионов нет цвета и запаха, а наличие отрицательных электронов на орбите позволяет им притягивать из воздуха различные микровещества. Анионы также удаляют из воздуха пыль и убивают микробы. Связь «анион-воздух» аналогична связи «витамин-пища». Именно поэтому анионы также называют «воздушными витаминами», «элементом долголетия» и «очистителем воздуха». Хотя полезные свойства анионов оставались долгое время в тени, они крайне важны для человеческого здоровья. Мы не можем позволить себе пренебрегать их целебными свойствами. Так, анионы могут аккумулировать и нейтрализовать пыль, уничтожать вирусы с положительно заряженными электронами, проникать в клетки микробов и уничтожать их, предотвращая, таким образом, негативные последствия для человеческого организма. Чем больше в воздухе анионов, тем меньше в нем микробов (когда же концентрация анионов достигает определенного уровня, то содержание микробов и вовсе сводится к нулю). Здоровье людей напрямую зависит от содержания анионов в воздухе. Если в попадающем в человеческое тело воздухе содержание анионов слишком низкое или, наоборот, слишком высокое, то человек начинает судорожно дышать, может почувствовать усталость, головокружение, головную боль или даже впасть в депрессию.
Все это поддается лечению при условии, что содержание анионов в поступающем в легкие воздухе составляет 1200 анионов на 1 кубический сантиметр. Если содержание анионов внутри жилых помещений повысить до 1500 анионов на 1 кубический сантиметр, то Ваше самочувствие сразу улучшится; Вы начнете работать с удвоенной энергией, повышая тем самым производительность труда.
Таким образом, анионы – это незаменимый помощник в укреплении человеческого здоровья и продлении жизни. Международная Организация Здравоохранения установила, что минимальное содержание анионов в свежем воздухе должно составлять 1000 анионов на 1 кубический сантиметр. При определенных условиях состояния окружающей среды (например, в горных областях) люди за всю жизнь могут ни разу не испытать воспаление внутренних органов. Как правило, такие люди живут долго и остаются здоровыми всю жизнь, что является результатом достаточного содержания анионов в воздухе.
Катионами называют положительно заряженные ионы.
Анионами называют отрицательно заряженные ионы.
В процессе развития химии понятия «кислота» и «основание» претерпели серьёзные изменения. С точки зрения теории электролитической диссоциации кислотами называют электролиты, при диссоциации которых образуются ионы водорода H + , а основаниями - электролиты, при диссоциации которых образуются гидроксид-ионы OH – . Эти определения в химической литературе известны как определения кислот и оснований по Аррениусу.
В общем виде диссоциацию кислот представляют так:
где A – - кислотный остаток.
Такие свойства кислот, как взаимодействие с металлами, основаниями, основными и амфотерными оксидами, способность изменять окраску индикаторов, кислый вкус и т. д., обусловлены наличием в растворах кислот ионов H + . Число катионов водорода, которые образуются при диссоциации кислоты, называют её основностью. Так, например, HCl является одноосновной кислотой, H 2 SO 4 - двухосновной, а H 3 PO 4 - трёхосновной.
Многоосновные кислоты диссоциируют ступенчато, например:
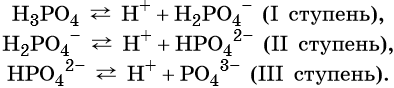
От образовавшегося на первой ступени кислотного остатка H 2 PO 4 – последующий отрыв иона H + происходит гораздо труднее из-за наличия отрицательного заряда на анионе, поэтому вторая ступень диссоциации протекает гораздо труднее, чем первая. На третьей ступени протон должен отщепляться от аниона HPO 4 2– , поэтому третья ступень протекает лишь на 0,001%.
В общем виде диссоциацию основания можно представить так:
где M + - некий катион.
Такие свойства оснований, как взаимодействие с кислотами, кислотными оксидами, амфотерными гидроксидами и способность изменять окраску индикаторов, обусловлены наличием в растворах OH – -ионов.
Число гидроксильных групп, которые образуются при диссоциации основания, называют его кислотностью. Например, NaOH - однокислотное основание, Ba(OH) 2 - двухкислотное и т. д.
Многокислотные основания диссоциируют ступенчато, например:
Большинство оснований в воде растворимо мало. Растворимые в воде основания называют щелочами .
Прочность связи М-ОН возрастает с увеличением заряда иона металла и увеличением его радиуса. Поэтому сила оснований, образуемых элементами в пределах одного и того же периода, уменьшается с возрастанием порядкового номера. Если один и тот же элемент образует несколько оснований, то степень диссоциации уменьшается с увеличением степени окисления металла. Поэтому, например, у Fe(OH) 2 степень основной диссоциации больше, чем у Fe(OH) 3 .
Электролиты, при диссоциации которых одновременно могут образовываться катионы водорода и гидроксид-ионы, называют амфотерными . К ним относят воду, гидроксиды цинка, хрома и некоторые другие вещества. Их полный перечень приведён в уроке 6, а их свойства рассмотрены в уроке 16.
Солями называют электролиты, при диссоциации которых образуются катионы металлов (а также катион аммония NH 4 +) и анионы кислотных остатков.

Химические свойства солей будут описаны в уроке 18.
Тренировочные задания
1. К электролитам средней силы относится
1) H 3 PO 4
2) H 2 SO 4
3) Na 2 SO 4
4) Na 3 PO 4
2. К сильным электролитам относится
1) KNO 3
2) BaSO 4
4) H 3 PO 4
3) H 2 S
3. Сульфат-ион в значительном количестве образуется при диссоциации в водном растворе вещества, формула которого
1) BaSO 4
2) PbSO 4
3) SrSO 4
4) K 2 SO 4
4. При разбавлении раствора электролита степень диссоциации
1) остается неизменной
2) понижается
3) повышается
5. Степень диссоциации при нагревании раствора слабого электролита
1) остается неизменной
2) понижается
3) повышается
4) с начала повышается, потом понижается
6. Только сильные электролиты перечислены в ряду:
1) H 3 PO 4 , K 2 SO 4 , KOH
2) NaOH, HNO 3 , Ba(NO 3) 2
3) K 3 PO 4 , HNO 2 , Ca(OH) 2
4) Na 2 SiO 3 , BaSO 4 , KCl
7. Водные растворы глюкозы и сульфата калия соответственно являются:
1) с ильным и слабым электролитом
2) неэлектролитом и сильным электролитом
3) слабым и сильным электролитом
4) слабым электролитом и неэлектролитом
8. Степень диссоциации электролитов средней силы
1) больше 0,6
2) больше 0,3
3) лежит в пределах 0,03-0,3
4) менее 0,03
9. Степень диссоциации сильных электролитов
1) больше 0,6
2) больше 0,3
3) лежит в пределах 0,03-0,3
4) менее 0,03
10. Степень диссоциации слабых электролитов
1) больше 0,6
2) больше 0,3
3) лежит в пределах 0,03-0,3
4) менее 0,03
11. Электролитами являются оба вещества:
1) фосфорная кислота и глюкоза
2) хлорид натрия и сульфат натрия
3) фруктоза и хлорид калия
4) ацетон и сульфат натрия
12. В водном растворе фосфорной кислоты H 3 PO 4 наименьшая концентрация частиц
1) H 3 PO 4
2) H 2 PO 4 –
3) HPO 4 2–
4) PO 4 3–
13. Электролиты расположены в порядке увеличения степени диссоциации в ряду
1) HNO 2 , HNO 3 , H 2 SO 3
2) H 3 PO 4 , H 2 SO 4 , HNO 2
3) HCl, HBr, H 2 O
14. Электролиты расположены в порядке уменьшения степени диссоциации в ряду
1) HNO 2 , H 3 PO 4 , H 2 SO 3
2) HNO 3 , H 2 SO 4 , HCl
3) HCl, H 3 PO 4 , H 2 O
4) CH 3 COOH, H 3 PO 4 , Na 2 SO 4
15. Практически необратимо диссоциирует в водном растворе
1) уксусная кислота
2) бромоводородная кислота
3) фосфорная кислота
4) гидроксид кальция
16. Электролитом, более сильным по сравнению с азотистой кислотой, будет
1) уксусная кислота
2) сернистая кислота
3) фосфорная кислота
4) гидроксид натрия
17. Ступенчатая диссоциация характерна для
1) фосфорной кислоты
2) соляной кислоты
3) гидроксида натрия
4) нитрата натрия
18. Только слабые электролиты представлены в ряду
1) сульфат натрия и азотная кислота
2) уксусная кислота, сероводородная кислота
3) сульфат натрия, глюкоза
4) хлорид натрия, ацетон
19. Каждое из двух веществ является сильным электролитом
1) нитрат кальция, фосфат натрия
2) азотная кислота, азотистая кислота
3) гидроксид бария, сернистая кислота
4) уксусная кислота, фосфат калия
20. Оба вещества являются электролитами средней силы
1) гидроксид натрия, хлорид калия
2) фосфорная кислота, азотистая кислота
3) хлорид натрия, уксусная кислота
4) глюкоза, ацетат калия
Химия - "волшебная" наука. А где вы еще получите безопасное вещество, соединив два опасных? Речь идет об обыкновенной поваренной соли - NaCl . Рассмотрим подробнее каждый элемент, опираясь на ранее полученные знания об устройстве атома.
Натрий - Na
, щелочной металл (группа IA).
Электронная конфигурация: 1s 2 2s 2 2p 6 3s 1
Как видим, натрий имеет один валентный электрон, который он "согласен" отдать, чтобы его энергетические уровни стали завершенными.
Хлор - Cl
, галоген (группа VIIA).
Электронная конфигурация: 1s 2 2s 2 2p 6 3s 2
3p 5
Как видим, хлор имеет 7 валентных электронов и ему "не хватает" одного электрона, чтобы его энергетические уровни стали завершенными.
Теперь догадываетесь, почему так "дружны" атомы хлора и натрия?
Ранее говорилось, что полностью "укомплектованные" энергетические уровни имеют инертные газы (группа VIIIA) - у них полностью заполнены внешние s и p-орбитали. Отсюда они так плохо вступают в химические реакции с другими элементами (им просто не надо ни с кем "дружить", поскольку ни отдавать, ни принимать электроны они "не хотят").
Когда валентный энергетический уровень заполнен - элемент становится стабильным или насыщенным .
Инертным газам "повезло", а что же делать остальным элементам периодической таблицы? Конечно же, "искать" себе пару, подобно дверному замку и ключу - определенному замку соответствует свой ключ. Так и химические элементы, пытаясь заполнить свой внешний энергетический уровень, вступают с другими элементами в реакции, создавая устойчивые соединения. Т.к. заполняются внешние s (2 электрона) и р (6 электронов) орбитали, то данный процесс получил название "правило октета" (октет = 8)
Натрий: Na
На внешнем энергетическом уровне атома натрия находится один электрон. Для перехода в стабильное состояние, натрий должен: либо отдать этот электрон, либо принять семь новых. Исходя из вышесказанного, натрий будет отдавать электрон. При этом у него "исчезает" 3s-орбиталь, а количество протонов (11) будет на один превосходить количество электронов (10). Поэтому, нейтральный атом натрия превратится в положительно заряженный ион - катион .
Электронная конфигурация катиона натрия: Na + 1s 2 2s 2 2p 6
Особо внимательные читатели справедливо скажут, что такая же электронная конфигурация и у неона (Ne). Так что же, натрий превратился в неон? Вовсе нет - не забывайте о протонах! Их по-прежнему; у натрия - 11; у неона - 10. Говорят, что катион натрия является изоэлектронным неону (поскольку их электронные конфигурации одинаковы).
Подведем итог:
- атом натрия и его катион отличаются одним электроном;
- катион натрия имеет меньший размер, поскольку он теряет внешний энергетический уровень.
Хлор: Cl
У хлора ситуация прямо противоположная - на внешнем энергетическом уровне у него находится семь валентных электронов и ему надо принять один электрон, чтобы стать стабильным. При этом произойдут следующие процессы:
- атом хлора примет один электрон и станет отрицательно заряженным анионом (17 протонов и 18 электронов);
- электронная конфигурация хлора: Cl - 1s 2 2s 2 2p 6 3s 2 3p 6
- анион хлора является изоэлектронным аргону (Ar);
- поскольку внешний энергетический уровень хлора "достроился", то радиус катиона хлора будет немного больше, чем у "чистого" атома хлора.
Поваренная соль (хлорид натрия): NaCl
Исходя из вышесказанного, видно, что электрон, который отдает натрий, становится электроном, который получает хлор.
В кристаллической решетке хлорида натрия каждый катион натрия окружен шестью анионами хлора. И наоборот, каждый анион хлора окружен шестью катионами натрия.
В результате перемещения электрона образуются ионы: катион натрия (Na +) и анион хлора (Cl -). Поскольку противоположные заряды притягиваются, то образуется устойчивое соединение NaCl (хлорид натрия) - поваренная соль .
В результате взаимного притяжения противоположно заряженных ионов, образуется ионная связь - устойчивое химическое соединение.
Соединения с ионными связями называют солями . В твердом состоянии все ионные соединения являются кристаллическими веществами.
Следует понимать, что понятие ионной связи довольно относительно, строго говоря к "чистым" ионным соединениям можно отнести только те вещества, у которых разность в электроотрицателности атомов, которые образуют ионную связь, равна или более 3. По этой причине в природе существует всего с десяток чисто ионных соединений - это фториды щелочных и щелочно-земельных металлов (например, LiF; относительная электроотрицательность Li=1; F=4).
Чтобы не "обижать" ионные соединения, химики договорились считать, что химическая связь является ионной, если разность электроотрицательностей атомов, образующих молекулу вещества равна или более 2. (см. понятие электроотрицательности).
Катионы и анионы
Другие соли образуются по аналогичному принципу, что и хлорид натрия. Металл отдает электроны, а неметалл их получает. Из периодической таблицы видно, что:
- элементы группы IA (щелочные металлы) отдают один электрон и образуют катион с зарядом 1 + ;
- элементы группы IIA (щелочноземельные металлы) отдают два электрона и образуют катион с зарядом 2 + ;
- элементы группы IIIA отдают три электрона и образуют катион с зарядом 3 + ;
- элементы группы VIIA (галогены) принимают один электрон и образуют анион с зарядом 1 - ;
- элементы группы VIA принимают два электрона и образуют анион с зарядом 2 - ;
- элементы группы VA принимают три электрона и образуют анион с зарядом 3 - ;
Распространенные одноатомные катионы
Распространенные одноатомные анионы
Не все так просто с переходными металлами (группа В), которые могут отдавать разное количество электронов, образуя при этом по два (и более) катиона, имеющих разные заряды. Например:
- Cr 2+ - ион двухвалентного хрома; хром (II)
- Mn 3+ - ион трехвалентного марганца; марганец (III)
- Hg 2 2+ - ион двухатомной двухвалентной ртути; ртуть (I)
- Pb 4+ - ион четырехвалентного свинца; свинец (IV)
Многие ионы переходных металлов могут иметь разную степень окисления.
Ионы не всегда бывают одноатомными, они могут состоять из группы атомов - многоатомные ионы . Например, ион двухатомной двухвалентной ртути Hg 2 2+ : два атома ртути связаны в один ион и имеют общий заряд 2 + (каждый катион имеет заряд 1 +).
Примеры многоатомных ионов:
- SO 4 2- - сульфат
- SO 3 2- - сульфит
- NO 3 - - нитрат
- NO 2 - - нитрит
- NH 4 + - аммоний
- PO 4 3+ - фосфат
В обычных условиях молекулы и атомы воздуха нейтральны. Однако при ионизации, которая может происходить посредством обычного излучения, ультрафиолетовой радиации или же посредством простого удара молнии, молекулы воздуха теряют часть вращающихся вокруг атомного ядра отрицательно заряженных электронов, которые в дальнейшем присоединяются к нейтральным молекулам, придавая отрицательный заряд. Такие молекулы мы и называем анионами. У анионов нет цвета и запаха, а наличие отрицательных электронов на орбите позволяет им притягивать из воздуха различные микрочастицы, удаляя таким образом из воздуха пыль и убивая микробы. Роль анионов в составе воздуха сопоставима со значением витаминов для питания человека. Именно поэтому анионы также называют «воздушными витаминами», «элементом долголетия» и «очистителем воздуха».
Хотя полезные свойства анионов оставалась долгое время в тени, они крайне важны для человеческого здоровья. Мы не можем позволить себе пренебрегать их целебными свойствами.
Так, анионы могут аккумулировать и нейтрализовать пыль, уничтожать вирусы с положительно заряженными электронами, проникать в клетки бактерий и уничтожать их, предотвращая, таким образом, негативные последствия для человеческого организма. Чем больше в воздухе анионов, тем меньше в нем микробов (когда же концентрация анионов достигает определенного уровня, то содержание микробов и вовсе сводится к нулю).
Содержание анионов в 1 кубическом сантиметре воздуха следующее: 40-50 анионов в жилых помещениях города, 100-200 анионов в городском воздухе, 700-1000 анионов в открытом поле и более 5000 анионов в горных долинах и лощинах. Здоровье людей напрямую зависит от содержания анионов в воздухе. Если в попадающем в человеческое тело воздухе содержание анионов слишком низкое, то человек начинает судорожно дышать, может почувствовать усталость, головокружение, головную боль или даже впасть в депрессию. Все это поддается лечению при условии, что содержание анионов в поступающем в легкие воздухе составляет 1200 анионов на 1 кубический сантиметр. Если содержание анионов внутри жилых помещений повысить до 1500 анионов на 1 кубический сантиметр, то ваше самочувствие сразу улучшится; вы начнете работать с удвоенной энергией, повышая тем самым производительность труда. Таким образом, анионы - это незаменимый помощник в укреплении человеческого здоровья и продления жизни.
Всемирная Организация Здравоохранения установила, что минимальное содержание анионов в свежем воздухе составляет 1000 анионов на 1 кубический сантиметр. При определённых условиях состояния окружающей среды (например, в горных областях), люди могут за всю жизнь не подвергнуться внутреннему воспалению или заражению. Как правило, такие люди живут долго и остаются здоровыми всю жизнь, что является результатом достаточного содержания анионов в воздухе.
В последние годы во всем мире возрос интерес к лечебным и гигиеническим свойствам анионов. После многолетних исследований сотрудники компании "Виналайт" ("WINALITE") (г. Шэньчжэнь) разработали уникальные прокладки лечебно-профилактического действия. Усовершенствовав обычные прокладки и встроив в них высокотехнологичные ионизаторы, мы получили национальный патент на производство данного вида продукции. Анионовый чип в прокладках "Love Moon " может генерировать до 5800 анионов на 1 кубический сантиметр; он эффективно устраняет бактерии и вирусы, способные привести к воспалению женской сферы (вагиниту), а также предотвращает их повторное появление.
Почти все женские болезни бывают вызваны анаэробными бактериями. Когда анионовый чип генерирует поток анионов высокой плотности, в то же время выделяется ионизированный кислород, который нейтрализует неблагоприятную анаэробную среду, активизирует работу ферментов, устраняет воспаление, нормализует кислотно-щелочной баланс. В то же время при нормальной температуре материал анионового чипа способен выделять полезные для человеческого организма магнитные волны длиной 4-14 микронов, интенсивностью свыше 90%, которые активируют молекулы воды в клетках, стимулируя процесс синтеза ферментов.
Таким образом, на основе исключительно физического воздействия, достигается эффект уничтожения бактерий и устранения неприятного запаха, что позволяет заботиться о женском здоровье с помощью высоких технологий.
Анионовые прокладки "











